实验室制取二氧化碳 原理、方法与注意事项
二氧化碳是一种无色、无味、密度比空气大的气体,在科学研究和工业生产中有着广泛的应用。在实验室中,我们通常采用简易且可控的方法来制取二氧化碳。本文将详细介绍其制取原理、常用方法、装置步骤以及重要的安全注意事项。
一、制取原理
实验室制取二氧化碳最经典的反应是利用碳酸钙(通常是大理石或石灰石的主要成分)与稀盐酸发生复分解反应。其化学反应方程式为:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑
选择此方法的原因在于:
- 原料易得且廉价(大理石、稀盐酸)。
- 反应速率适中,易于控制和收集气体。
- 反应条件温和,在常温下即可进行。
需要注意的是,不宜使用稀硫酸与碳酸钙反应,因为生成的微溶硫酸钙会覆盖在大理石表面,阻碍反应的进一步进行。
二、实验装置与步骤
1. 实验装置
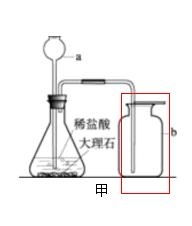
通常采用“固液常温型”发生装置,即使用锥形瓶(或广口瓶)与长颈漏斗(或分液漏斗,便于控制反应)、导管等组装而成。收集方法采用向上排空气法,因为二氧化碳的密度(约1.977 g/L)大于空气的平均密度。
2. 操作步骤
- 检查气密性:连接好发生装置后,将导管末端浸入水槽,用手捂住锥形瓶,观察导管口是否有气泡冒出,确保装置不漏气。
- 添加药品:先在锥形瓶中放入适量大理石碎块,然后从长颈漏斗中加入稀盐酸,液面需浸没漏斗下端管口(形成液封,防止气体逸出)。
- 收集气体:将导管通入集气瓶底部,利用二氧化碳密度大的特性,将空气从瓶口向上排出。用燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳已收集满。
- 停止反应:反应结束后,可将导气管移出液面,或关闭分液漏斗活塞,使反应停止。
三、注意事项与安全
- 安全第一:盐酸具有腐蚀性,操作时应佩戴护目镜和手套,避免皮肤或眼睛直接接触。
- 气密性检查:实验前必须检查装置气密性,否则无法有效收集气体。
- 液封要求:使用长颈漏斗时,务必确保其下端管口浸没在液面以下,防止气体从漏斗逸出。
- 收集验满:二氧化碳不支持燃烧,验满时用燃着的木条置于瓶口即可,切勿伸入瓶内。
- 废物处理:反应后的废液(主要含氯化钙和过量盐酸)应倒入指定的废液缸,进行中和处理后再排放,符合环保要求。
四、二氧化碳的性质与检验
制得的二氧化碳可用于后续的性质实验:
- 物理性质:观察其颜色、状态,并通过倾倒熄灭蜡烛火焰的实验证明其密度比空气大。
- 化学性质:
- 不支持燃烧:将二氧化碳通入燃有阶梯蜡烛的烧杯中,下层蜡烛先熄灭。
- 与水反应:通入紫色石蕊试液,试液变红(生成碳酸,不稳定)。
- 与澄清石灰水反应:通入澄清石灰水,溶液变浑浊(生成白色碳酸钙沉淀),这是检验二氧化碳的常用方法,反应方程式为:CO₂ + Ca(OH)₂ → CaCO₃↓ + H₂O。
实验室制取二氧化碳是一项基础且重要的化学实验。通过掌握其原理、规范操作流程并严格遵守安全注意事项,我们不仅能成功制得所需气体,还能深入理解相关的化学原理和实验思维,为后续的科学探索打下坚实基础。
如若转载,请注明出处:http://www.xjyqrq.com/product/22.html
更新时间:2026-05-07 13:53:43